Propriedades Periódicas
As propriedades periódicas são características dos elementos químicos que variam de maneira previsível com base em sua posição na Tabela Periódica. Estas propriedades refletem a estrutura eletrônica dos átomos dos elementos e influenciam seu comportamento químico e físico. Aqui estão algumas das principais propriedades periódicas:
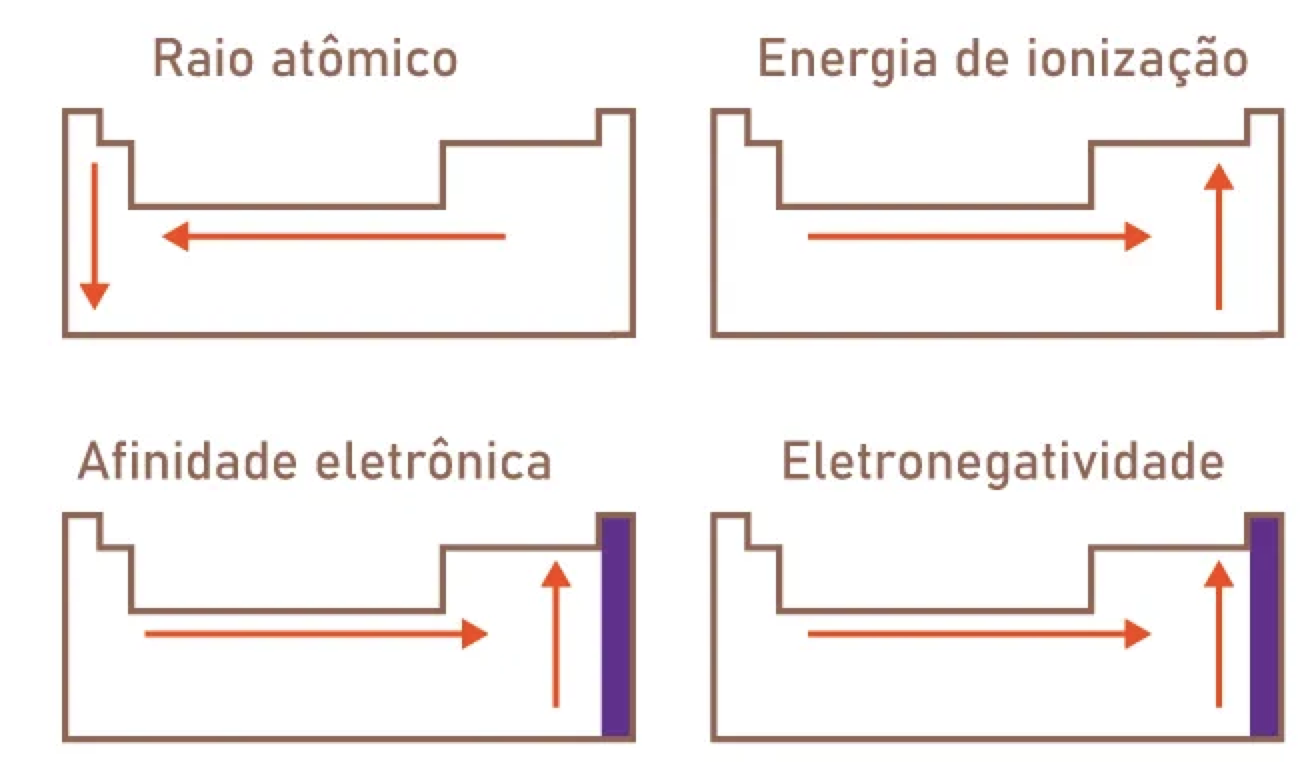
- Raio Atômico: Refere-se ao tamanho de um átomo. Geralmente, o raio atômico aumenta de cima para baixo em um grupo (coluna) devido ao aumento do número de camadas eletrônicas, e diminui da esquerda para a direita em um período (linha) devido ao aumento da carga nuclear efetiva, que atrai os elétrons para mais perto do núcleo.
- Energia de Ionização: É a energia necessária para remover um elétron de um átomo no estado gasoso. A energia de ionização aumenta da esquerda para a direita em um período, devido ao aumento da carga nuclear efetiva, e diminui de cima para baixo em um grupo, pois os elétrons mais externos estão mais distantes do núcleo e são menos fortemente atraídos.
- Afinidade Eletrônica: Também chamada de eletroafinidade, refere-se à energia liberada, quando é introduzido um elétron. A afinidade eletrônica geralmente aumenta da esquerda para a direita em um período e diminui de cima para baixo em um grupo.
- Eletronegatividade: É uma medida da tendência de um átomo atrair um par de elétrons numa ligação química. A eletronegatividade aumenta da esquerda para a direita ao longo de um período e diminui de cima para baixo em um grupo. O flúor é o elemento mais eletronegativo.
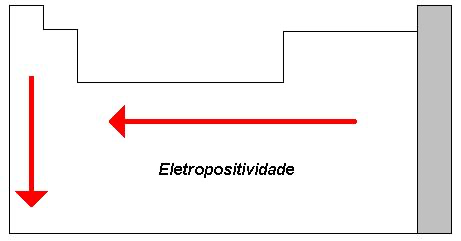
- Caráter Metálico: Refere-se à tendência de um elemento exibir propriedades metálicas, como condutividade elétrica e brilho. É a propriedade inversa a eletronegatividade. O caráter metálico aumenta de cima para baixo dentro de um grupo e diminui da esquerda para a direita ao longo de um período.
Cada uma dessas propriedades é influenciada pela configuração eletrônica dos elementos e pela estrutura geral da Tabela Periódica, que é organizada em função do número atômico dos elementos.
